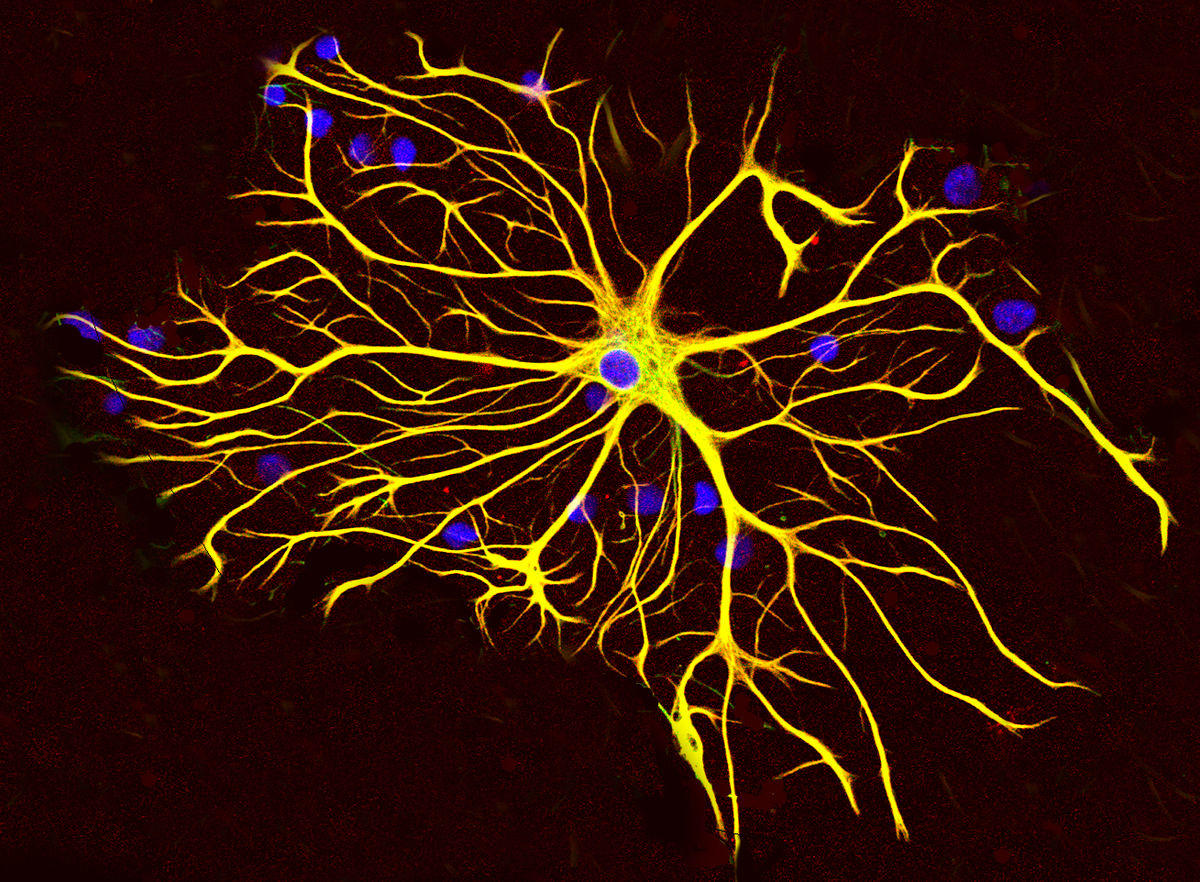
Astrosit hücre gövdesi 10–20 μm uzunluğundadır ve süreçleri 20–30 μm’ye yayılarak astrosit glial hücreleri oluşturur. Yıldız şeklindeki hücresinin bu yıldız şekli, ışık mikroskobu görüntüsünde en net şekilde görülebilir.
Astrositler, hipokampusun CA1 bölgesindeki yayılan katmanın hacminin %4 ila 8’ini kaplar ve bu da onları en yaygın glial alt tip yapar. Astrositlere ek olarak. Hipokampus, mikroglia ve oligodendrositler dahil olmak üzere diğer glial hücrelere ev sahipliği yapar.
Sinapsların yakınında astrositlerin varlığı, sinaptik işlev için önemli görünmektedir (aşağıya bakınız). Fare hipokampüsünün bu elektron mikroskobu görüntülemesinde sinaptik kompleksleri (oklar) ile yakından tanımlanmış astrositler (mavi) görülebilir.
Astrositler, en üst düzeyde yapısal özelliklerle tanımlanabilir:
• Düzensiz, yıldız şeklinde
• Birçok glikojen granülü
• Ara iplik demetleri olarak
• Nispeten berrak sitoplazma durumunda
Diğer glial alt tipler gibi, astrositlerin de beyin işlevinin temel bileşenleri olan nöronlar için yalnızca destek ve bakım hücreleri olarak hizmet ettiği düşünülmektedir. Bununla birlikte, son birkaç yılda yapılan araştırmalar, astrositler için sinaptik iletişimde olduğu kadar sinaptik olmayan iletişimde de çok daha merkezi bir rol olduğunu göstermiştir.
Sinaptik iletimde astrositler, hücre dışı boşluktaki iyonların, nörotransmiterlerin, nöromodülatörlerin ve enerji kaynaklarının boyutunu, bileşimini ve konsantrasyonlarını modüle ederek bir etki gösterebilir. Astrositlerin mesaj iletimine dahil olması, muhtemelen sadece sinaptik öncesi ve sonrası ortakları değil, aynı zamanda komşu glia’yı da içeren, sinaptik birimin yeniden değerlendirilmesine izin verir.
İçindekiler
Astral hücresel: dolaşmayan bir iletişim aracı
Sinaptik olmayan haberciler olarak, astrositler sinirde sinsityal stellat adı verilen bir ağ oluşturur. Moleküllerin sinsityuma difüzyonu, astrositler arasındaki boşluk bağlantılarından gerçekleşir.
Çalışmalar, kalsiyum dalgalarının sinsitya yoluyla yayıldığını (Cornell Bell ve diğerleri, 1990) ve bu dalgaların mekanik stimülasyon ve nörotransmitter glutamat tarafından indüklenebileceğini bulmuştur. Kalsiyum dalgaları, ağ üzerinden astrositlere kalsiyum akışı kalsiyuma duyarlı salınıma, iyon alımına ve nöromodülatörlere neden olursa, kompleksin uzun mesafeli modülasyonuna ve hücre dışı boşlukta moleküllerin konsantrasyonuna yol açabilir. Astral sinsityum, beyin içinde sinaptik olmayan bir iletişim aracı sağlar. Astrositler, hücre dışı boşluk ve kan damarları içindeki yapı hakkında bilgi almanın yanı sıra, birçok sinapstan gelen bilgileri aynı anda algılayabilir ve entegre edebilir. Astrositler, nöronların aksine amplifiye edilemez.
Nöronlar için metabolik faktörlerin sağlanması
Astrositlerin sinaptik fonksiyona katılmasının bir yolu, nöronal aktivite için metabolitler sağlamaktır. Beynin ana enerji kaynağı olan glikoz, kan damarlarıyla temas eden astrositlerle merkezi sinir sistemine girer. Kan damarlarıyla temas eden yıldız şeklindeki süreçler, yıldız şeklindeki bacaklar olarak bilinir.
Kanıtlar, glikozun kısmen astrositler tarafından metabolize edildiğini ve ara ürünlerin nöronal kullanım için salındığını göstermektedir (Pfrieger ve Barres, 1996; Tsacopoulos ve Magistretti, 1996). Hipokampüste, glial metabolizma, Krebs döngüsünün glial-spesifik bir inhibitörü olan florositrat tarafından bloke edildiğinde sinaptik iletim bloke edilir (Keyser ve Pellmar, 1994; Pfrieger ve Barres, 1996). Bu, nöronların sinaptik işlev için gereken yakıt için glial hücrelere bağlı olduğu anlamına gelir. Ek olarak, kanıtlar glia tarafından nöronlara iletilen yakıt miktarının sinaptik aktivite miktarına bağlı olduğunu göstermektedir. Bir bulguya göre, glutamat astrositik glikoz alımını ve ardından hücre dışı boşluğa laktat salınımını uyarır (Pellerin ve Magistretti, 1994; Pfrieger ve Barres, 1996).
Astrositik şişlik ve filopodia uzantısı ile değiştirilmiş ECS hacim fraksiyonu
Astrositler, hücre dışı boşluğun hacim fraksiyonunun önemli bir belirleyicisidir. Astrosit şişmesinin glutamat ve adenozin reseptörlerinin uyarılması sonucu meydana geldiği gösterilmiştir (Hansson, 1994; Bourke ve ark. 1983). Mitokondral dilatasyon veya hipertrofi, glutamatın astrositlere fokal olarak uygulanmasıyla indüklenebilir (Cornell Bell ve diğerleri, 1992). Bu ipliksi uzantı, astrosit boyutunu ve morfolojisini değiştirebilir ve muhtemelen hücre dışı boşluk tarafından işgal edilen hacim fraksiyonunu da değiştirebilir.
Sinaptik fonksiyon, hücre dışı hacim fraksiyonuna duyarlıdır. Hacim fraksiyonu azaldıkça, hücre dışı boşluğun bileşenlerinin konsantrasyonu artar ve bu teorik olarak nöronların verilen belirli bir miktarda nörotransmitere tepkisini artırır. Gerçekten de, astrositlerin şişmesine neden olduğu bilinen artan K+ konsantrasyonunun bir sonucu olarak hücre dışı hacim fraksiyonu azaldığında, nöronal uyarılabilirliğin nöbetlerin meydana geldiği noktaya kadar arttığı gösterilmiştir (Porter ve ark. McCarthy, 1997; Traynelis ve Dingledine , 1989). Ayrıca, astrosit şişmesini önlediği bilinen furosemidin son zamanlarda elektrik kaynaklı nöbetleri önlediği gösterilmiştir (Hochman ve diğerleri, 1995; Porter ve McCarthy, 1997).
İyon kanalları ve nörotransmiter reseptörleri
Astrositler çeşitli iyon kanalları, nörotransmiter reseptörleri ve taşıyıcılar içerir. Astrositler, beynin bu iyonlarla olan dengesini korumak için K+ ve Ca2+ iyon kanallarını kullanır. Sinaptik aktivite sırasında, hücre dışı boşlukta astrositik alımla azalan bir K+ birikimi vardır (Nilsson ve Hagberg, 1997). Astrositler daha sonra alınan K+’yı kılcal kana salgılarlar (Nilsson ve Hagberg, 1997). Ca2+ astrositler için iyon kanallarının rolü henüz net değil.
İyon kanallarına ek olarak, astrositler nörotransmiter reseptörleri içerir. 1980’den önce (Van Calker ve Hamprecht, 1980), bu reseptörler sadece nöronlarda gözleniyordu ve astrositlerde olduğu düşünülmüyordu. Astrositlerde bulunan reseptör tipleri, nöronlarda bulunanlara benzer. Astrositik reseptörler, her biri astrositler arasında ve farklı beyin bölgelerinde farklı şekilde ifade edilen ve her biri ikinci bir haberci zincirle bağlanan glutamat, gababrik, adrenerjik, serotonerjik ve muskarinik reseptörleri içerir (Kimelberg, 1995; revize edilmiş; Porter ve McCarthy, 1997).
Nöronların uyarılabilirliğini etkileme olasılıkları
Hücre boyutunu değiştirmenin yanı sıra astrositler, nöronal uyarılabilirliği modüle etmenin başka yollarına da sahiptir. Örneğin, astrositin presinaptik terminal yakınında depolarizasyonu, salınan nörotransmiterlerin miktarını artırabilir (Ronback ve Hanson, 1997). Ayrıca donör salınımı Ca bağımlı ise, hücre dışı boşlukta Ca konsantrasyonunun astrositik kontrolü uyarılabilirlikte değişikliklere yol açacaktır (Ronnback ve Hansson, 1997). Başka olasılıklar da var. Nitekim araştırmalar, kültürde gelişen nöronların, etki mekanizması bilinmeyen glial hücreler ortaya çıkana kadar tam olarak işlevsel sinapslara ulaşmadığını göstermiştir (Pfrieger ve Barres, 1997).
Astrositik glutamat alımı ve sinaptik glutamat yayılma potansiyeli
Astrositler, hücre dışı glutamat konsantrasyonlarını subtoksik seviyelerde tutmak için kritik olan yüksek afiniteli glutamat taşıyıcıları içerir, böylece nöronal hücre ölümünü önler (Rothstein ve diğerleri, 1994; Rothstein ve diğerleri, 1996). Taşıyıcılar tarafından yetersiz glutamat alımının amyotrofik lateral skleroz, Alzheimer hastalığı, şizofreni ve AIDS’te rolü olduğu düşünülmektedir. Glutamat alımı, muhtemelen sinaptik sinyallemeyi sonlandırarak, glutamatın sinaptik yarıkta geçici seyrini de modüle edebilir (Minrick ve Zoromsky, 1994). Ek olarak, astrositler sentetik glutamat eliminasyonuna aracılık edebilir.
Yukarıda açıklanan, NMDA (N) reseptörlerinin damlacıkları neden AMPA (A) reseptörlerinden farklı algıladığını açıklayan varsayımsal bir modeldir. Noktalı çizgi, glutamatın 1. sinaps yarığından kaçıp 2. sinapsa ulaştığı yolu gösterir. Bu modelde, bağlı olduğu glutamat alım yolu boyunca astrositik (siyah) bir işlemin olmaması nedeniyle difüzyon gerçekleşir. (Karanlık) sinaps 2’nin boğulması, çok az glutamat salınımına neden olur veya hiç olmaz, bu nedenle, sinaps 2’ye ulaşan glutamat konsantrasyonu yalnızca (yüksek afiniteli) NMDA reseptörlerini aktive etmek için yeterlidir. Bu modeldeki sorun, yüksek düzeyde ekstrasinaptik glutamatın genel toksisiteye yol açmasıdır.
Astrositler, kendilerinden glutamat difüzyonunu etkili bir şekilde bloke etmek için yeterince yüksek konsantrasyonlarda glutamat taşıyıcılara sahip olduğundan, sinapsların yakınında astrositlerin varlığı, difüzyonun meydana gelip gelmediğinin önemli bir belirleyicisi olabilir. CA1 hipokampüsünde, glutamat alımı için herhangi bir örtüşen yapı olmaksızın kısa sinaptik mesafeler gözlemlenmiştir (Ventura ve Harris, 1999). Alternatif olarak, astrositler salınan glutamata doğru büyüdüğünde (Cornell Bell ve diğerleri, 1990), sinapsların yalnızca aksonal ve omurga arayüzlerinde astrosit süreçleri yoluyla glutamat salgılaması mümkündür.
Yukarıda açıklanan, NMDA (N) reseptörlerinin damlacıkları neden AMPA (A) reseptörlerinden farklı algıladığını açıklayan alternatif bir modeldir. (A)’daki Sinaps 2, çok az öncü glutamat sentaz salgılar veya hiç serbest bırakmaz ve yalnızca NMDA reseptörleri sinaptiktir. Sinaps 2, bir miktar glutamatı otomatik olarak inhibe ettiğinde, NMDA reseptörleri bunu algılar, ancak glutamatı tespit edecek AMPA reseptörleri yoktur. (a)’daki sinaps 2’deki salınım miktarı, aktif sinaps 1’den yeni ortaya çıkan sinaps 2’ye doğru kaymayı önlemek için bitişik sinapslar ve astrositler (siyah) üzerine yayılmak için yetersizdir. Eşzamanlı olarak, sinaps 2, postsinaptik AMPA reseptörlerini işe alır.
Astrosit büyüme modeli/AMPA reseptörü alım modeli olan bu model, difüzyona karşı çıkar. Alternatif olarak, NMDA ve AMPA reseptörleri tarafından algılanan kanal sayısındaki tutarsızlık, sinaps aktif hale geldiğinde AMPA reseptörlerinin postsinaptik yoğunluğa alınmasıyla açıklanabilir (Malenka ve Nicoll, 1995’te gözden geçirilmiştir).
kaynak:
Britanya
yazar: Tuncay Bayraktar
Diğer gönderilerimize göz at
[wpcin-random-posts]